EL ACIDO GALICO PROVENIENTE DE LA TARA
Extracción de Taninos (ácido gálico) a partir del Polvo de Vaina de Tara (Caesalpinia Spinosa)
Los taninos vegetales son productos naturales que tienen la capacidad de formar complejos con proteínas. Dentro de este contexto, son los productos naturales más importantes usados industrialmente en los procesos que transforman las pieles en cueros. Caracterizaremos los taninos utilizados (evaluación de su poder curtiente) y partiendo de una formulación base en función del artículo final elegido (capellada de calzado) se realiza el curtido.
La Tara (Caesalpinia spinosa)
fruto en vainas delgas con pepas, esta materia prima en su cascara contiene un
alto contenido de taninos por lo que esta investigación estudió los factores
que afectan en la etapa de extracción para la concentración de taninos (Ácido
Gálico) a partir de la cascara de tara en polvo.
El ácido gálico es un ácido de
tipo orgánico, de color amarillo claro, cuyo nombre según nomenclatura
corresponde a 3,4,5-trihidroxibenzoico, su fórmula molecular es C7H6O5, su peso
molecular es 170,12 [g/mol], se encuentra hojas de té, corteza de roble y otras
plantas. También está presente en las agallas, que corresponden a estructuras inducidas
por insectos, hongo o bacterias en plantas.
El ácido gálico puede formar
sales y esteres que son denominados galatos, debido a que se hace referencia a las
agallas que es donde principalmente se encuentran, de ahí proviene su nombre.
También se puede encontrar tanto en su forma libre como formando parte de
taninos (metabolitos secundarios de las plantas, empleados para trabajar el
cuero).
El ácido gálico es obtenido
mediante la hidrólisis de ácido tánico con ácido sulfúrico o enzima. Cuando se
calienta por encima de 220 C, el ácido gálico pierde dióxido de carbono para
formar pirogalol (C6H3 OH3), que se utiliza en la producción de colorantes
azoicos y reveladores fotográficos y en los laboratorios para la absorción de
oxígeno.
1. Propiedades:
a. Físicas:
ü
Punto de fusión: 253ºC
ü
Densidad a 40ºC: 1.694 g/cc
ü
Constante de disociación (25ºC): 3.8*10-5
ü
Calor de combustión: 633.7 Kcal/mol
ü
Solubilidad: una parte de ácido gálico se
disuelve en:
o 85p.
agua 20ºC
o 3p.
agua caliente
o 6
p. alcohol
o 12
p. glicerina
o 5
p. acetona
o 100
p. éter
ü Insoluble en: cloroformo, benceno y bencina
b. Químicas:
La química del ácido gálico
pertenece a la del grupo carboxílico, oxidrilos y de las posiciones no
sustituidas en el anillo, algunas reacciones implican más de un grupo
funcional. De las reacciones químicas más importantes tenemos:
ü
Reacción de oxidación
ü
Reacción por condensación
ü
Reacción por descarboxilacion
ü
Reacciones por sustitución
ü Reacciones por esterificación y eterificación
ü Reacciones por reducción
2. Aplicaciones:
En la industria farmacéutica (por ejemplo, en síntesis de trimetoprim) de otro modo como sustancia patrón (o de referencia) se usa para determinar el contenido de fenoles en diferentes compuestos de interés, mediante el reactivo de Folin-Ciocalteu (FRC); el cual es una mezcla de fosfomolibdato y fosfotungstato que detecta antioxidantes de tipo fenólicos, funciona midiendo la cantidad de sustancia analizada que es necesaria para inhibir la oxidación del reactivo.
Por otra parte también se puede utilizar para sintetizar mescalina (que es un alcaloide alucinógeno), para hacer antioxidantes utilizados en los alimentos Alimentar a las industrias, y los tintes de tinta en la fabricación de papel fotográfico.
Usados industrialmente en los procesos que transforman las pieles en cueros, dentro de los artículos fabricados por curtido o recurtido vegetal se pueden citar suela, capellada, plantilla y forro para calzado, cueros para tapicería, para marroquinería entre otros.
Las normas que aplican para los análisis y especificaciones para los mismos en este caso vinculado al calzado, son una recopilación de distintos organismos y empresas más importantes del ramo, siendo en última instancia una relación comercial que estima los estándares de calidad de las materias primas para la industria del calzado, prendas y tapicería. El organismo que regula las normas de cueros es la IULTCS (Unión Internacional de Sociedades de Técnicos del Cuero) entidad internacional que esta formada por todas las asociaciones que corresponden a los diferentes países socios.
2. Derivados:
El ácido gálico se utiliza como importante sustrato para la síntesis de galato de propilo, antioxidante de uso en la industria alimentaria. Además es usada en la manufactura de pirogallol y como resina fotosensible en la producción de semiconductores. El Pirogalol se utiliza en la tinción de pieles y cuero, y en el develado de fotografías, a su vez, tras la depolimerización de pirogalol se pueden producir adhesivos.
a. Pirogalol (CAS 87-66-1)
El Pirogalol es
producido quimicamente hacienda reaccionar al ácido gálico en presencia de 6 N
HCl (Zeida et al., 1998). En la actualidad, la conversion biologicas de ácido
gálico usando la enzima ácido gálico descarboxilasa, producida a partir de la
inmovilización de microorganismos, está siendo intensivamente investigada. A
través estos procesos biológicos, se logra una mayor especifidad en la
extracción de derivados gálicos, así como la disminución de la contaminación
ambiental causada por las sales formadas en la síntesis química.
b. Galato de Propilo (CAS 12-17-99)
Se obtiene a
partir de la síntesis del propanol y del ácido gálico. La bioconversion del
galato de propilo.
Usos:
ü Antioxidante en productos grasos, especialmente añadido para prevenir la rancidez.
ü Su uso está restringido en los alimentos. Ampliamente usado en los cosméticos.
ü La ingesta máxima diaria es de 1.4 mg/kg de peso corporal
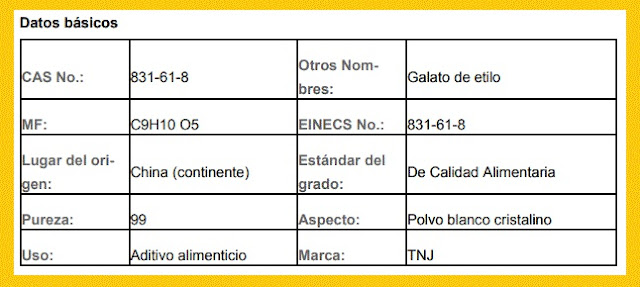
c. Galato de Etilo (CAS 831-61-8)
Especificaciones:
·
Aspecto: polvo blanco cristalino
·
Sinónimos: Éster de etilo ácido de Gallice, EG. , Galato de etilo
·
Nombre químico: Etilo -3, 4, trihydroxybenzoate 5
·
Mol. Forma y Mol. Peso: C9H10O5 = 198.2
Descripción:
Inodoro. Levemente soluble en agua. Soluble en etanol y éter. Prácticamente
insoluble en aceite del cacahuete.
Especificaciones para cumplir con los requisitos de la
edición BP1998:
·
Punto de fusión: 151-154 centígrado
·
Cloruro: ≤ 330ppm
·
Pérdida en la sequedad: ≤ 1.0%
·
Ceniza sulfatada: ≤ 0.1%
Aplicaciones: Se
utiliza como antioxidante de preparaciones medicinales y bioquímicas






0 comentarios:
Publicar un comentario